未来のクリーンエネルギー「水素」を自分の手で生み出そう!(水素の発生実験)
サイエンストレーナーの桑子研です。毎日が実験。
「燃えると水になるクリーンな気体」、そんな魔法のような物質を聞いたことがありますか?実はそれ、水素のことなんです。今回は、そんな未来のエネルギーともいわれる水素を、身近な材料を使って発生させる、ドキドキの化学実験に挑戦してみましょう!
水素の発生実験に挑戦!
今回は、亜鉛と塩酸を使って水素を発生させる実験です。前の時間には酸素の発生実験もやっているので、性質の違いを比べてみるのも面白いですよ。
まずは準備から!
水素を発生させるには、以下の材料と器具を使います。
材料
•亜鉛(花状、小さな粒状のもの)1g •10%塩酸 7mL

器具
•試験管 2本 •マッチ •燃え差し(火が消えたけどまだ熱いもの) •濡れ雑巾(万が一の安全対策!)
水素を集める手順
① 水素を発生させる!

試験管にうすい塩酸を入れ、そこに花状亜鉛を加えます。すると…細かい泡がシュワシュワと元気に発生!この気体こそが、今回の主役、水素です。この反応は、化学の世界では次のように表せます。
Zn (亜鉛) + 2HCl (塩酸) ⟶ ZnCl₂ (塩化亜鉛) + H₂ (水素)
亜鉛が塩酸に溶けることで、塩化亜鉛という物質に変化し、同時に水素が発生するのです。発生した水素は、水上置換法という方法で試験管に集めます。気泡の出が悪い冬場などは、試験管をお湯で少し温めてあげると反応が活発になりますよ。

一年前に一度使った亜鉛を入れてもしっかりと反応が起こりました!
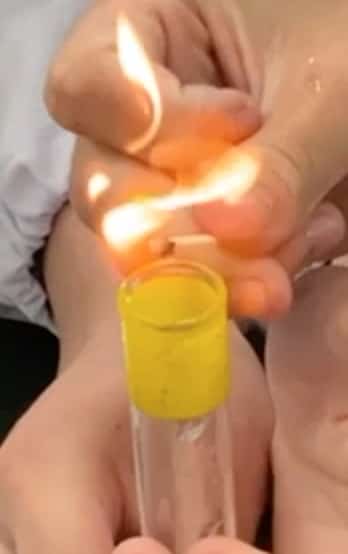
② 火を近づけてみよう!
集めた水素に、火のついたマッチを近づけてみましょう。(※1本目は空気が混じっている可能性があるので、2本目の試験管を使いましょう!)さて、ここでクイズ!火を近づけると、どうなると思いますか?
正解は……「ポンッ!」と小さな爆発音を立てて燃えるんです!
これは、水素が空気中の酸素と激しく反応(燃焼)して、水(H₂O)に変化した証拠。この音は、反応のエネルギーで周りの空気が一瞬でふくらんだことで鳴る、いわば「ミニチュア版の爆発音」なのです。実際にやってみると、「シュボッ!」とか「ヒュン!」とか、条件によって音が変わるのも面白い発見ですよ。
③ さらに実験!
もしもう1本水素が溜まったら、試験管に石灰水を加えて振ってみましょう。酸素の実験では石灰水に変化はありませんでしたが、今回はどうでしょうか?…おそらく、変化はないはずです。石灰水が白くにごるのは二酸化炭素の性質なので、水素や酸素とは違うことがわかりますね。
科学の深掘り:不思議な亜鉛の謎
今回使ったのは「花状亜鉛」。実は、亜鉛の形によって水素の発生しやすさが全く違います。同じ亜鉛なのに、なぜでしょう?
ヒントは「表面積」!
例えば、角砂糖と粉砂糖、どちらが水に速く溶けるか想像してみてください。すぐに溶けるのは粉砂糖ですよね。それは、粉砂糖の方が水に触れる面積(表面積)が広いからです。
これと同じで、複雑な形をした花状亜鉛は、ツルツルの粒状亜鉛よりも塩酸に触れる面積が広いため、反応がたくさん起こり、勢いよく水素が発生するのです。こうした「なぜだろう?」を考えるのが、科学の醍醐味ですね!実験後の亜鉛は、表面の光沢がなくなり黒っぽく変身します。これは、亜鉛が溶けだしたり、表面に別の物質ができたりするためです。もし再利用するなら、やすりがけをしてピカピカの面を出す必要があります。

左:実験前 右:実験後
まとめ
生徒たちは器具の扱いにもすっかり慣れ、1時間で手際よく実験を進めることができました。その成長ぶりに感動です!身の回りの現象も、化学の目で見ると新しい発見がたくさんあります。ぜひ、次の「なぜ?」を探してみてください。
お問い合わせ・ご依頼について
科学の不思議やおもしろさをもっと身近に!自宅でできる楽しい科学実験や、そのコツをわかりやすくまとめています。いろいろ検索してみてください!
・科学のネタ帳の内容が本になりました。詳しくはこちら
・運営者の桑子研についてはこちら
・各種ご依頼(執筆・講演・実験教室・TV監修・出演など)はこちら
・記事の更新情報はXで配信中!
![]() 科学のネタチャンネルでは実験動画を配信中!
科学のネタチャンネルでは実験動画を配信中!
6月のイチオシ実験!
レモンやオレンジで風船を割ろう!インパクトが抜群のリモネン風船の実験

テレビ番組監修・イベント等のお知らせ
- 6月3日(水)20:30〜 「
バカリズムのちょっとバカりハカってみた!」(テレビ東京)を科学監修・出演します。テーマは「 そばの出前は何人前まで運べるのか、限界を測ってみた」です。 - 6月4日(木) 7:00〜 「THE突破ファイル」(日本テレビ)について科学監修しました。
- 6月14日(日) 千葉大学インスタレーション「探究」にて講師を務めます
- 6月26日(金) 公開研究会「脱作業化!デジタル化と段階的指導で実現する オームの法則の探究」
- 6月28日(日) ダビンチマスターズ@昭和女子
- 7月18日(土) 教員向け実験講習会「ナリカカサイエンスアカデミー」の講師をします。お会いしましょう。
書籍のお知らせ
- 『大人のための高校物理復習帳』(講談社)…一般向けに日常の物理について公式を元に紐解きました。特設サイトでは実験を多数紹介しています。※増刷がかかり6刷となりました(2026/02/01)

- 『きめる!共通テスト 物理基礎 改訂版』(学研)… 高校物理の参考書です。イラストを多くしてイメージが持てるように描きました。授業についていけない、物理が苦手、そんな生徒におすすめです。特設サイトはこちら。

各種SNS(更新情報をお届け!)
X(Twitter)/instagram/Facebook(日本語)
Explore
- 楽しい実験…お子さんと一緒に夢中になれるイチオシの科学実験を多数紹介しています。また、高校物理の理解を深めるための動画教材も用意しました。
- 理科の教材… 理科教師をバックアップ!授業の質を高め、準備を効率化するための選りすぐりの教材を紹介しています。
- Youtube…科学実験等の動画を配信しています。
- 科学ラジオ …科学トピックをほぼ毎日配信中!AI技術を駆使して作成した「耳で楽しむ科学」をお届けします。
- 講演 …全国各地で実験講習会・サイエンスショー等を行っています。
- About …「科学のネタ帳」のコンセプトや、運営者である桑子研のプロフィール・想いをまとめています。
- お問い合わせ …実験教室のご依頼、執筆・講演の相談、科学監修等はこちらのフォームからお寄せください。


