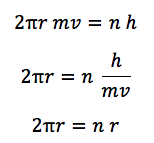なぜ電子は落ち込まないの?ボーアの量子条件の式
公式をそのまま暗記するのはつまらない!この公式は何なのか?どのように使うのか?公式これだけ!シリーズ、今日は「量子条件の式」について、簡単に見て行きましょう。
量子条件の式は、ラザフォードの原子模型の問題である、水素が原子核に落ち込んでしまう問題を解決するために、ボーアが作った仮設です。ボーアが発表した当初の1913年では、次のような数式になっていました。
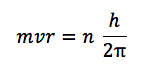
ここにド・ブロイの発見した物質波長(ドブロイ波長)の式、λ=h/mvを入れると、
上記の式になります。この式の意味は、電子はその物質波の波長の整数倍の起動しかとることができないという意味があります。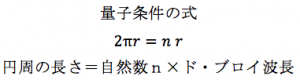
nに1,2,3といれていくと、
2πr=λ
2πr=2λ
2πr=3λ
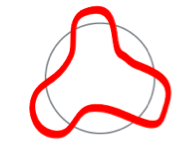
となります。左辺の半径rは波長によってすこしずつ大きな軌道をとるということになりまふね!たとえば3λの場合、
例)
n=3(手書きで下手くそですみません(^^;))
整数倍にならない波については、何回もその軌道を回っていると波同士で打ち消し合ってしまい、存在できないと考えました。
化学のk殻、m殻、l殻のように、電子がある決まった軌道をとるのは、ド・ブロイ波長と関係があるのですね!
原子分野も面白い(^^)
ニュースレター
・ニュースレターはブログでは載せられない情報を配信しています。
[subscribe2]