酸とアルカリが出会ったら?目に見える化学のドラマ「中和の結晶」を作ろう(塩酸と水酸化ナトリウムを使った中和実験)
サイエンストレーナーの桑子研です。毎日が実験。
突然ですが、みなさんは「酸っぱさ」と「苦さ」という正反対の性質が出会うと、何が起こるか想像できますか? 理科の世界では、強烈な個性を持つ物質同士が手を取り合い、お互いの力を打ち消し合う中和という不思議なドラマが起こります。今回は、その反応の結果として現れる「目に見える化学の足跡」――美しい結晶を作るワクワクの実験をご紹介します。シンプルな材料で、色の変化を楽しみながら科学の奥深さを体験してみましょう!

まずは準備から!成功の鍵は「正確な濃度」
実験を成功させるためには、料理と同じで「下ごしらえ」が肝心です。 材料として使うのは、酸性の代表である「塩酸」と、アルカリ性の代表である「水酸化ナトリウム」の0.1mol/L水溶液です。
ここで少しだけ、濃度計算のお話をしましょう。 0.1mol/Lという濃度は、反応が急激すぎず、かつ色の変化がはっきりとわかる、中学生の実験にぴったりの「ちょうどいい濃さ」なんです。
今回の準備では、少し多めの480mLの水に塩酸を4mL加えました。また、水酸化ナトリウムは、水500mLに2gを溶かして用意しました。これで4クラス分(10班×4クラス)の実験準備がバッチリ整います。
実験スタート!魔法のように色が変わる瞬間
① 塩酸に「酸性の色」をつける
まず、100mLのビーカーにピペットで塩酸10mLを入れます(1クラス分の場合、あらかじめ100mLビーカーに10mL入れておきます)。この時、ビーカーの下に白い紙を敷いておくと、色の変化が劇的にわかりやすくなりますよ。 そこにBTB溶液を5滴くらいたらすと、一瞬で鮮やかな黄色に!これは溶液が「酸性」であることを示しています。

溶液が黄色に!
ピペットの使い方は、指先の繊細なコントロールが必要です。理科の基本スキルなので、ここでしっかり練習しておきましょう。
② 中和反応の tug-of-war(綱引き)
次に、水酸化ナトリウム水溶液を2mLずつ加えて、ガラス棒でゆっくり混ぜていきます。

写真は準備の様子。白が水酸化ナトリウム、赤が塩酸です。
あらかじめ塩酸は4mLずつ、水酸化ナトリウムは14mLずつ試験管に入れておきます。(1クラス分の場合)
最初は黄色だった溶液が、水酸化ナトリウムを入れるたびに一瞬青くなり、また黄色に戻ります。10mLほど入れたあたりで、ついに溶液が青色に!これは「アルカリ性」に傾いた証拠。ゴールである「中和点」がすぐそこまで来ている合図です。

いき過ぎた!
③ 微調整が最高に楽しい!「完璧な緑色」を目指せ
青くなってしまったら、ここからは本当の勝負です。 塩酸を1滴ずつ慎重に加え、中性を示す「緑色」になるよう調整します。
「あ、また黄色になった!」「今度は青すぎる!」
この行ったり来たりの微調整が、実はこの実験で一番盛り上がるポイントです。絶妙なバランスでピタッと美しい緑色になった瞬間、あちこちの班から歓声が上がります。早い班なら約10分でこの「奇跡の緑」に到達できます。

完成!

最後のお楽しみ―ミクロの宝石「結晶観察」
中和が無事に終わったら、仕上げの作業です。 スライドガラスにその溶液を1滴垂らし、そのまま水を蒸発させます。すると、どうでしょう……。 次回の授業で顕微鏡をのぞくと、そこには四角い、透明な美しい結晶が現れているはずです!
自分のプレパラートに番号を振っておくと便利です。
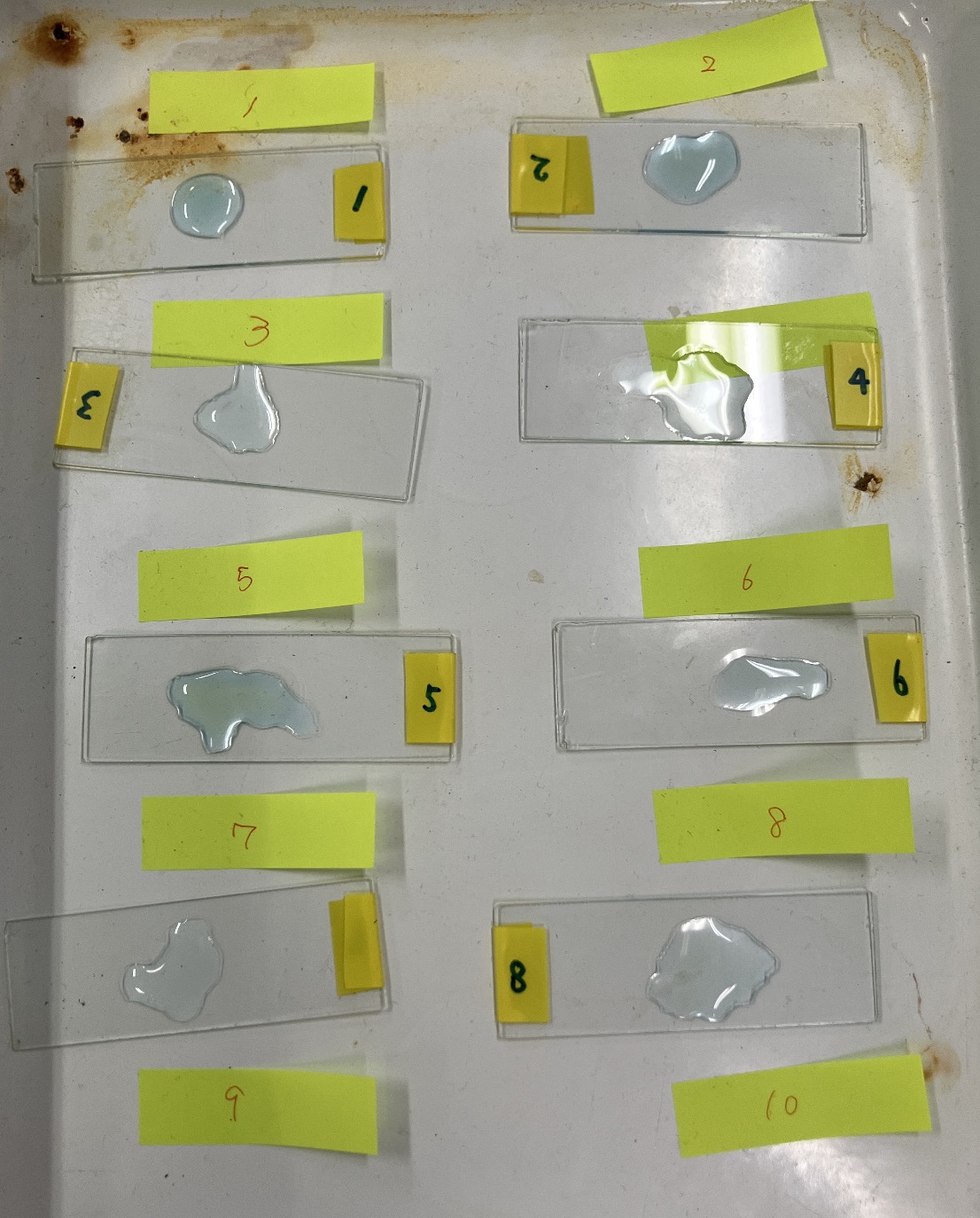
次の時間に観察となりますが、予備実験等でプレパラートを事前に作っておくと、同じ時間にまず確認で見れるのでおすすめです。
この正体は、私たちがよく知っている「食塩(塩化ナトリウム)」です。酸とアルカリが結びつき、全く別の物質へと姿を変えた証拠なのです。規則正しく並んだ立方体の姿は、まるでミクロの世界の宝石のようですね。
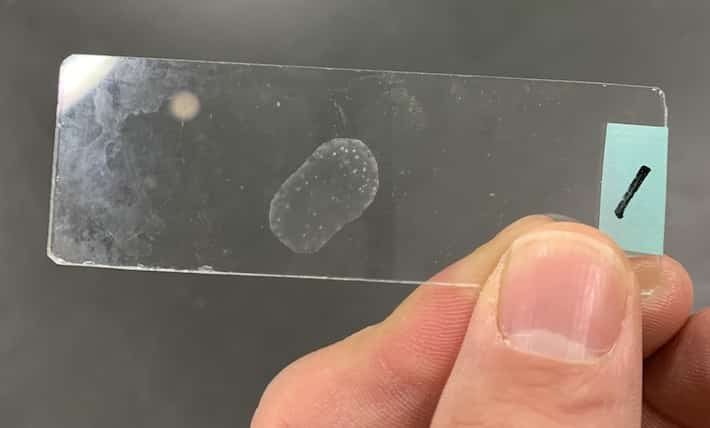


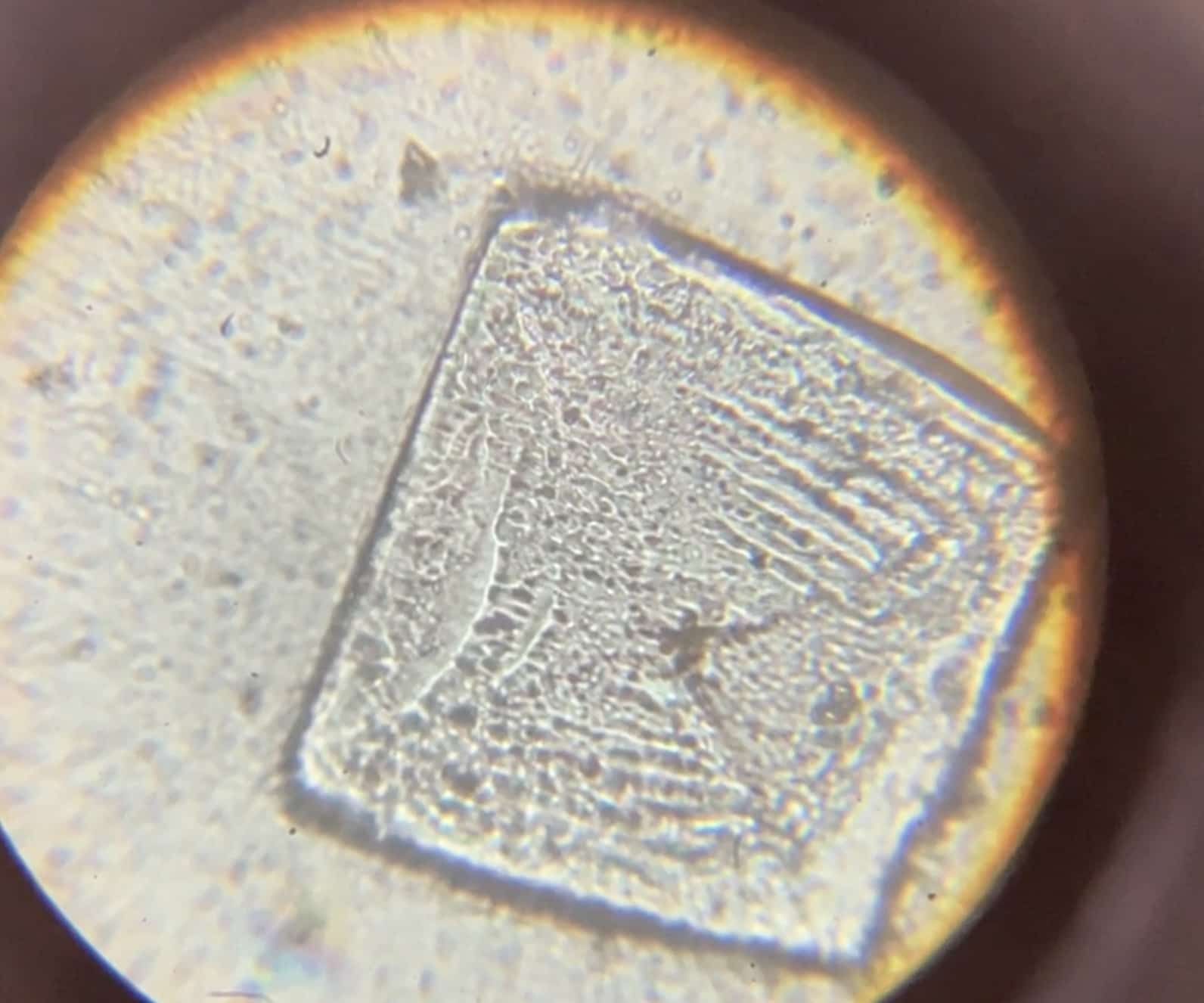
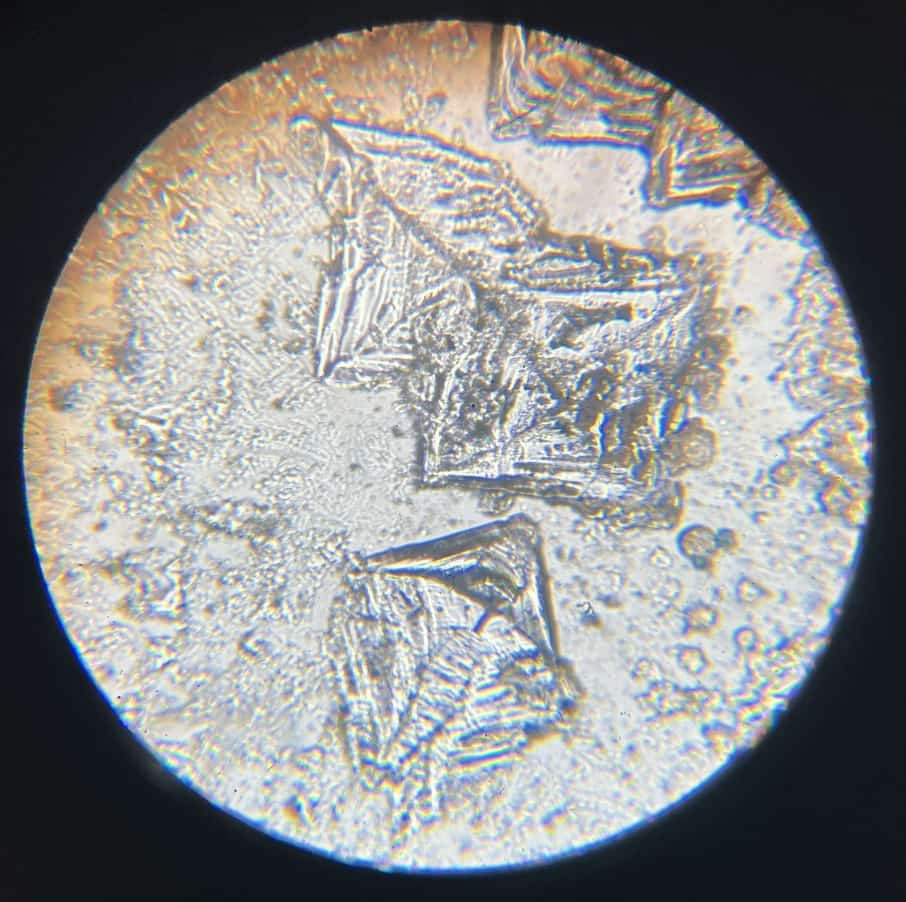
中には水酸化ナトリウムらしき樹状の結晶がみられることもあります。

色の鮮やかな変化を楽しみながら、化学の基本である「中和反応」を学び、最後には結晶観察までできるこの実験。 準備には少しコツがいりますが、生徒たちの驚きと発見に満ちた表情を見ると、理科教師として「やってよかった!」と心から思える瞬間です。みなさんもぜひ、この「色の魔法」と「結晶の輝き」を体験して、理科の楽しさを肌で感じてみてくださいね!
お問い合わせ・ご依頼について
科学の不思議やおもしろさをもっと身近に!自宅でできる楽しい科学実験や、そのコツをわかりやすくまとめています。いろいろ検索してみてください!
・科学のネタ帳の内容が本になりました。詳しくはこちら
・運営者の桑子研についてはこちら
・各種ご依頼(執筆・講演・実験教室・TV監修・出演など)はこちら
・記事の更新情報はXで配信中!
![]() 科学のネタチャンネルでは実験動画を配信中!
科学のネタチャンネルでは実験動画を配信中!
5月のイチオシ実験!
キーンと冷えるドライアイス!気温が上がってくるこの時期・ドライアイスを使った昇華・凝結・等速度直線運動の実験はいかが?

液体ゼロ!ドライアイスが消えるまでの3時間を科学する(昇華・凝結・等速度直線運動)
テレビ番組監修・イベント等のお知らせ
- 4月30日(木)「THE突破ファイル」(日本テレビ)の科学監修を担当しました。
- 5月8日(金)理科教育ニュースを担当しました。
- 6月14日(日) 千葉大学インスタレーション「探究」にて講師を務めます
- 6月26日(金) 千葉大学の公開研究会(中学理科について授業公開予定)
- 7月18日(土) 教員向け実験講習会「ナリカカサイエンスアカデミー」の講師をします。お会いしましょう。
書籍のお知らせ
- 『大人のための高校物理復習帳』(講談社)…一般向けに日常の物理について公式を元に紐解きました。特設サイトでは実験を多数紹介しています。※増刷がかかり6刷となりました(2026/02/01)

- 『きめる!共通テスト 物理基礎 改訂版』(学研)… 高校物理の参考書です。イラストを多くしてイメージが持てるように描きました。授業についていけない、物理が苦手、そんな生徒におすすめです。特設サイトはこちら。

各種SNS(更新情報をお届け!)
X(Twitter)/instagram/Facebook(日本語)
Explore
- 楽しい実験…お子さんと一緒に夢中になれるイチオシの科学実験を多数紹介しています。また、高校物理の理解を深めるための動画教材も用意しました。
- 理科の教材… 理科教師をバックアップ!授業の質を高め、準備を効率化するための選りすぐりの教材を紹介しています。
- Youtube…科学実験等の動画を配信しています。
- 科学ラジオ …科学トピックをほぼ毎日配信中!AI技術を駆使して作成した「耳で楽しむ科学」をお届けします。
- 講演 …全国各地で実験講習会・サイエンスショー等を行っています。
- About …「科学のネタ帳」のコンセプトや、運営者である桑子研のプロフィール・想いをまとめています。
- お問い合わせ …実験教室のご依頼、執筆・講演の相談、科学監修等はこちらのフォームからお寄せください。


