염산·황산·암모니아·염화구리의 희석 방법! 희석의 기본과 올바른 실험 준비법
과학 트레이너 쿠와코 켄입니다. 매일매일이 실험!

과학실에서 약품을 다룰 때, “안전하게, 정확하게, 효율적으로” 실험을 진행하기 위해서는 희석에 대한 기본 지식이 필수적입니다. 이번에는 약품 사용 시 알아두어야 할 희석 방법, 안전성 그리고 실제 실험에서의 농도 기준을 선생님들을 위해 정리해봤습니다. 원래 제가 궁금해서 찾아보고 정리한 내용인데, “꼼꼼하게 준비했다”는 것은 마음을 놓게 하는 요소가 되며, 실패 없는 준비가 수업의 질을 높여줍니다. 이 글을 읽으시면 자주 사용하는 약품의 희석에 대한 개념을 확실히 정리하실 수 있을 거예요.
예를 들어 하마지마 서점의 과학 편람 243페이지 등을 보면, 희석 방법에 대한 제조법 등이 정리되어 있습니다. 수산화나트륨의 전기 분해에 사용할 때 농도는 5%도 괜찮습니다. 염산의 전기 분해에 사용할 염산의 농도도 5%면 충분하다는 것을 알 수 있죠. 이 페이지에서는 더욱 자세하게, 현장 선생님들을 위해 실제 용액 제조법을 정리했습니다. 실제 질량 퍼센트 농도에서 몰 농도로 변환하는 방법 등의 계산 방법에 대해서는 다른 글에 정리해두었으니, 이쪽을 참고해주세요.
염산의 희석에 대하여
중학교 과학 실험에서 자주 사용하는 염산은 진한 염산을 한 번에 묽혀서 사용하는 것이 좋다고 합니다. 10% 염산을 만들려면 부피비로 진한 염산 1에 물 3.2를 더하면 됩니다. 예를 들어 500㎤의 진한 염산 전부를 10%로 만들려면 1600㎤의 물로 희석하는 것이 좋으므로, 3리터짜리 폴리에틸렌 용기(amazon)에 묽혀서 보관하면 편리합니다.

|
|
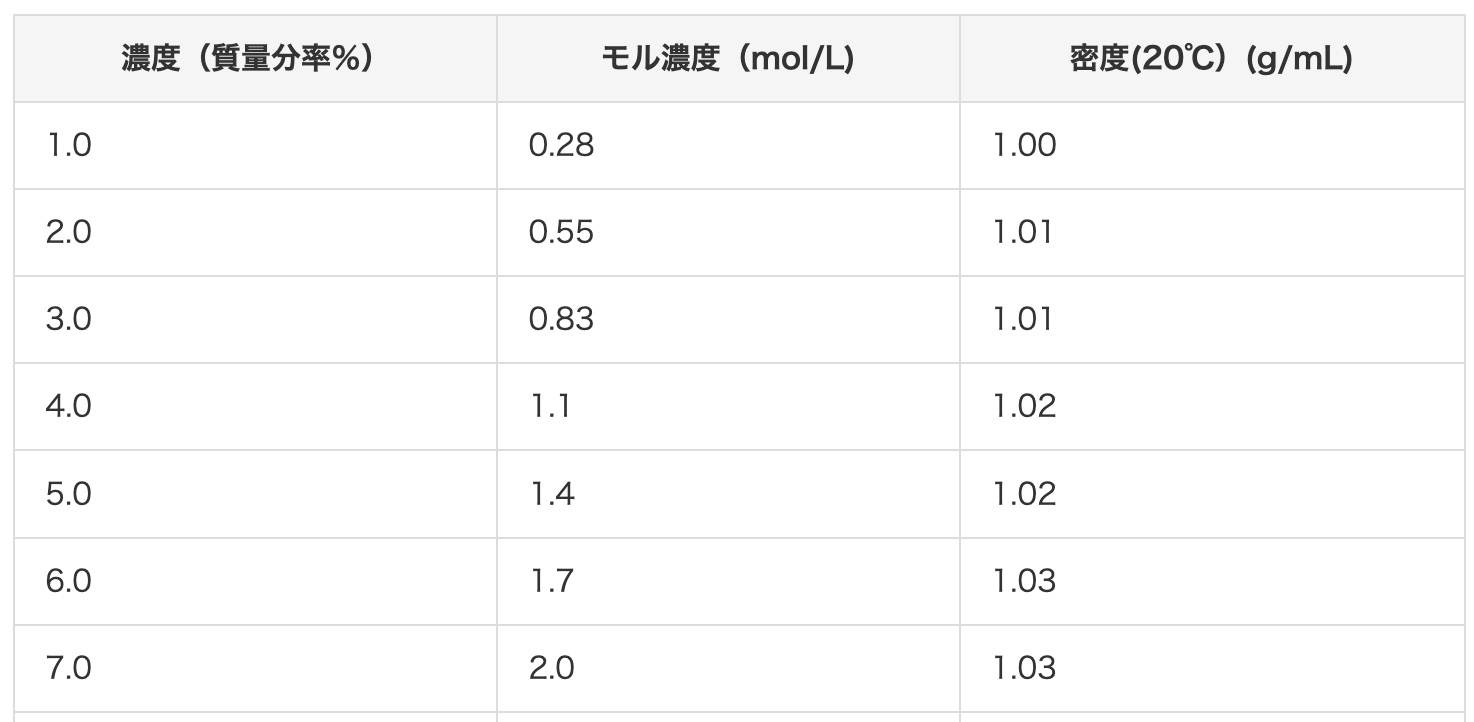
또한 희석 방법에 대해서는 이곳을 참고해주세요.
걱정되시는 분들은 식으로도 확인해보세요.
예를 들어 진한 염산은 12mol/L이고 밀도는 1.18g/mL이므로, 진한 염산 1L(1000mL) 용액의 질량은 다음과 같습니다.
1.18 × 1000 = 1180g
또한, 용질의 질량은 분자량을 36.5로 하면,
12 × 36.5 = 438g
따라서 진한 염산의 질량 퍼센트 농도는,
438 / 1180 = 37.1%
입니다. 이 농도를 물을 더해 10%로 만들려면, 더하는 물의 양을 x[g]이라고 할 때,
438 / (1180 + x) = 10 / 100
x = 3200g
이 됩니다. 따라서 염산 1L에 물 3.2L를 더하면 농도가 10%인 염산이 됩니다. 염산이 500mL라면 그 절반이므로 1.6L가 됩니다.
주의할 점
염산을 희석할 때는 물에 염산을 추가해야 합니다. 산이나 알칼리에 물을 추가하면 (X) 용해로 인한 발열로 인해 추가된 물이 튀어 오를 수 있기 때문입니다. 염산이나 황산의 희석 방법 등에 대한 참고 사이트를 정리해 두었습니다. 참고로 진한 염산의 농도와 진한 황산의 농도 차이는 용해도 차이 때문이라고 합니다.

농도 9%인 경우, 노르말 농도 N은 약 2.6 (2.6mol/L)
농도 4%인 경우, 노르말 농도 N은 약 1 (1mol/L)
참고: http://www.keins.city.kawasaki.jp/9/ke9004/benrihp060821/2020.benrichou.ensan.pdf
진한 염산의 농도는 12mol/L이다. 따라서 1mol/L 농도로 만들려면 12배 희석해야 한다. 총량이 12이고 그 안에 염산이 1이므로, 염산 1 : 물 11의 비율로 섞는 것이 좋다.
※주의 희석할 때, 산이나 알칼리에 물을 넣으면 용해로 인한 발열로 인해 첨가한 물이 튀어 위험할 수 있다. 희석할 때는 반드시 물에 산이나 알칼리를 넣도록 한다.
【염산의 경우】
・ 진한 염산의 농도는 12mol/L이다. 따라서 1mol/L 농도로 만들려면 12배 희석해야 한다. 총량이 12이고 그 안에 염산이 1이므로, 염산 1 : 물 11의 비율로 섞는 것이 좋다.
(예) 물 110mL에 염산 10mL를 넣는다.
※주의 희석할 때, 산이나 알칼리에 물을 넣으면 용해로 인한 발열로 인해 첨가한 물이 튀어 위험할 수 있다. 희석할 때는 반드시, 물에 산이나 알칼리를 넣도록 한다.
【암모니아수의 경우】
・ 진한 암모니아수는 14mol/L이다. 따라서 1mol/L 암모니아수를 만들 때는 진한 암모니아수 1 : 물 13의 비율로 섞는 것이 좋다.
※ 용질이 액체이면 몰 농도, 고체인 경우에는 분자량을 알면 목적하는 농도의 수용액을 만들 수 있다.참고 http://www.edu.pref.kagoshima.jp/curriculum/rika/shou/syougakkou2/gihouhtm/01page/page03.htm
수산화나트륨의 희석에 대하여
【수산화나트륨의 경우】
・ 수산화나트륨 1몰은 40g이다. 따라서 수산화나트륨 40g을 물에 녹여 1L로 만들었을 때가 1mol/L이다.
1mol/L (4%) 수산화나트륨 수용액 100mL를 만들려면 수산화나트륨 4g을 물에 녹여 100mL로 만든다.
※ 수산화나트륨은 물에 녹일 때 발열 반응을 일으킨다. 따라서 소량의 물에 녹여 수온을 올린 다음 나머지를 녹이면 쉽다.참고 http://www.edu.pref.kagoshima.jp/curriculum/rika/shou/syougakkou2/gihouhtm/01page/page03.htm
◆ 다량의 용액 (약 500mL 이상)을 만들 경우
만들 용량에 맞는 메스실린더(예: 500mL를 만들려면 500mL 또는 1000mL)로 증류수를 측정하여, 절반은 큰 비커 A에 옮기고 나머지는 메스실린더에 남겨둡니다.
저울을 사용하여 다른 비커 B에 수산화나트륨을 측정하여 즉시 1번 비커 A의 증류수에 넣고 잘 저어줍니다. 2번 비커 B 바닥에 붙어있는 수산화나트륨은 메스실린더의 증류수를 더하여 녹인 후 1번 비커 A에 옮깁니다.
필요하다면 시약 병에 옮겨 보관합니다. 시약 이름, 농도, 제조일, 제조자 등을 기재한 라벨을 붙여주세요.
◆ 소량의 용액 (약 500mL 미만)을 만들 경우
메스실린더(예: 100mL를 만들려면 100mL 또는 200mL)로 증류수를 측정합니다.
저울을 사용하여 비커에 수산화나트륨을 측정하여 즉시 1번에서 측정했던 증류수를 넣고 잘 저어줍니다.
필요하다면 시약 병에 옮겨 보관합니다. 시약 이름, 농도, 제조일, 제조자 등을 기재한 라벨을 붙여주세요.
염화구리 전기분해 시 농도 조절에 대하여
전기 분해에 사용할 염화구리 용액 조절은 염화구리 13g을 취해 증류수를 넣고 300g의 수용액으로 만들었습니다. 대략 3% 염화구리 수용액입니다. 자세한 내용은 이쪽을 참고해주세요. 묽은 용액이지만 실험은 충분히 가능합니다.
다니엘 전지 농도 조절에 대하여
#황산아연 수용액 5% 9.8g에 물 100g #황산구리 수용액 약 17% 35.7g에 물 100g
자세한 내용은 여기에 정리했습니다.
기타 참고할 만한 사이트
*산성·알칼리성 조사 실험 이 실험은 리트머스 종이의 색이 변하면 되므로, 보통 약 0.3~1 mol/L 정도면 충분합니다. 0.3 mol/L라면, 진한 염산 : 물 = 1:39 *금속을 넣어 수소 발생 실험 금속을 녹이는 실험은 어느 정도의 농도가 필요합니다. 약 3 mol/L로 묽히십시오. 진한 염산 : 물 = 1:3
참고 https://www.ice.or.jp/nc/?action=common_download_main&upload_id=1169
◆마지막으로
“조금 너무 진했나…”, “더 묽혀야 했을까?” 하는 불안감은 사전 지식과 준비로 해소할 수 있습니다. 희석 방법을 제대로 익혀두면 실험 시 안전성도 높아지고, 학생들에게 올바른 과학적 태도를 전달하는 데도 도움이 됩니다. 약품 취급에 충분히 주의하면서 과학의 즐거움과 깊이를 계속 전해나가도록 해요!
문의 및 의뢰에 대하여
과학의 신비와 재미를 더욱 가까이! 집에서 할 수 있는 즐거운 과학 실험과 그 노하우를 알기 쉽게 정리했습니다. 이것저것 검색해보세요!
・운영자 쿠와코 켄에 대해서는 여기
・각종 의뢰 (집필, 강연, 실험 교실, TV 자문, 출연 등)는 여기
・기사 업데이트 정보는 X에서 실시간 확인!
![]() 과학 꿀팁 채널에서는 실험 영상을 시청 중! (구독해주세요!)
과학 꿀팁 채널에서는 실험 영상을 시청 중! (구독해주세요!)
5月のイチオシ実験!
キーンと冷えるドライアイス!気温が上がってくるこの時期・ドライアイスを使った昇華・凝結・等速度直線運動の実験はいかが?

液体ゼロ!ドライアイスが消えるまでの3時間を科学する(昇華・凝結・等速度直線運動)
テレビ番組監修・イベント等のお知らせ
- 4月30日(木)「THE突破ファイル」(日本テレビ)の科学監修を担当しました。
- 5月8日(金)理科教育ニュースを担当しました。
- 6月14日(日) 千葉大学インスタレーション「探究」にて講師を務めます
- 6月26日(金) 千葉大学の公開研究会(中学理科について授業公開予定)
- 7月18日(土) 教員向け実験講習会「ナリカカサイエンスアカデミー」の講師をします。お会いしましょう。
書籍のお知らせ
- 『大人のための高校物理復習帳』(講談社)…一般向けに日常の物理について公式を元に紐解きました。特設サイトでは実験を多数紹介しています。※増刷がかかり6刷となりました(2026/02/01)

- 『きめる!共通テスト 物理基礎 改訂版』(学研)… 高校物理の参考書です。イラストを多くしてイメージが持てるように描きました。授業についていけない、物理が苦手、そんな生徒におすすめです。特設サイトはこちら。

各種SNS(更新情報をお届け!)
X(Twitter)/instagram/Facebook(日本語)
Explore
- 楽しい実験…お子さんと一緒に夢中になれるイチオシの科学実験を多数紹介しています。また、高校物理の理解を深めるための動画教材も用意しました。
- 理科の教材… 理科教師をバックアップ!授業の質を高め、準備を効率化するための選りすぐりの教材を紹介しています。
- Youtube…科学実験等の動画を配信しています。
- 科学ラジオ …科学トピックをほぼ毎日配信中!AI技術を駆使して作成した「耳で楽しむ科学」をお届けします。
- 講演 …全国各地で実験講習会・サイエンスショー等を行っています。
- About …「科学のネタ帳」のコンセプトや、運営者である桑子研のプロフィール・想いをまとめています。
- お問い合わせ …実験教室のご依頼、執筆・講演の相談、科学監修等はこちらのフォームからお寄せください。

![[상품 가격에 관해서는 링크가 생성된 시점과 현재 시점에 정보가 변경될 수 있습니다.] [상품 가격에 관해서는 링크가 생성된 시점과 현재 시점에 정보가 변경될 수 있습니다.]](https://hbb.afl.rakuten.co.jp/hgb/2c6a2576.25faaa1b.2c6a2577.0abda625/?me_id=1240371&item_id=10000489&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fnagamineshouten%2Fcabinet%2Fporikan%2F3-1.jpg%3F_ex%3D80x80&s=80x80&t=picttext)

