【不再搞混!】質量百分濃度與莫耳濃度自由轉換的化學秘方(規定度N・ppm)
我是科學訓練師 桑子研。每一天都是實驗!
你在看食譜時,看到「鹽少許」是不是總會困惑到底是多少呢?其實,在化學的世界裡,也有好幾種表示「濃度」的方式,科學家們會根據不同情況來選擇使用。這次,讓我們一起來探索兩種在理科實驗中常見的濃度單位:「質量百分濃度」和比較專業的「莫耳濃度」,看看它們之間要怎麼換算。學會了這個計算,你會發現化學世界變得更貼近生活,實驗也會變得更有趣、更安全喔!
如果想了解實際的稀釋方法,可以點這裡看看。
濃度的基本概念:了解單位的不同
國中課本裡最常用的是 「質量百分濃度」,但在實驗手冊或學術論文中,「莫耳濃度」 才是主流。所以,現在就讓我們來學會這兩種濃度的自由換算吧!只要掌握了計算方法,就會覺得超方便,而且實驗起來也更安心。
不論是質量百分濃度還是莫耳濃度,它們的基本概念都是一樣的:
溶質(溶在裡面的東西) ÷ 溶液(全部)
唯一的差別就在於它們使用的 「單位」。質量百分濃度用的是質量(公克)。
溶質(g) ÷ 溶液(g)
而莫耳濃度則是以化學反應中粒子的數量為依據,使用莫耳(mol)和體積(公升) 。
溶質(mol) ÷ 溶液(L)
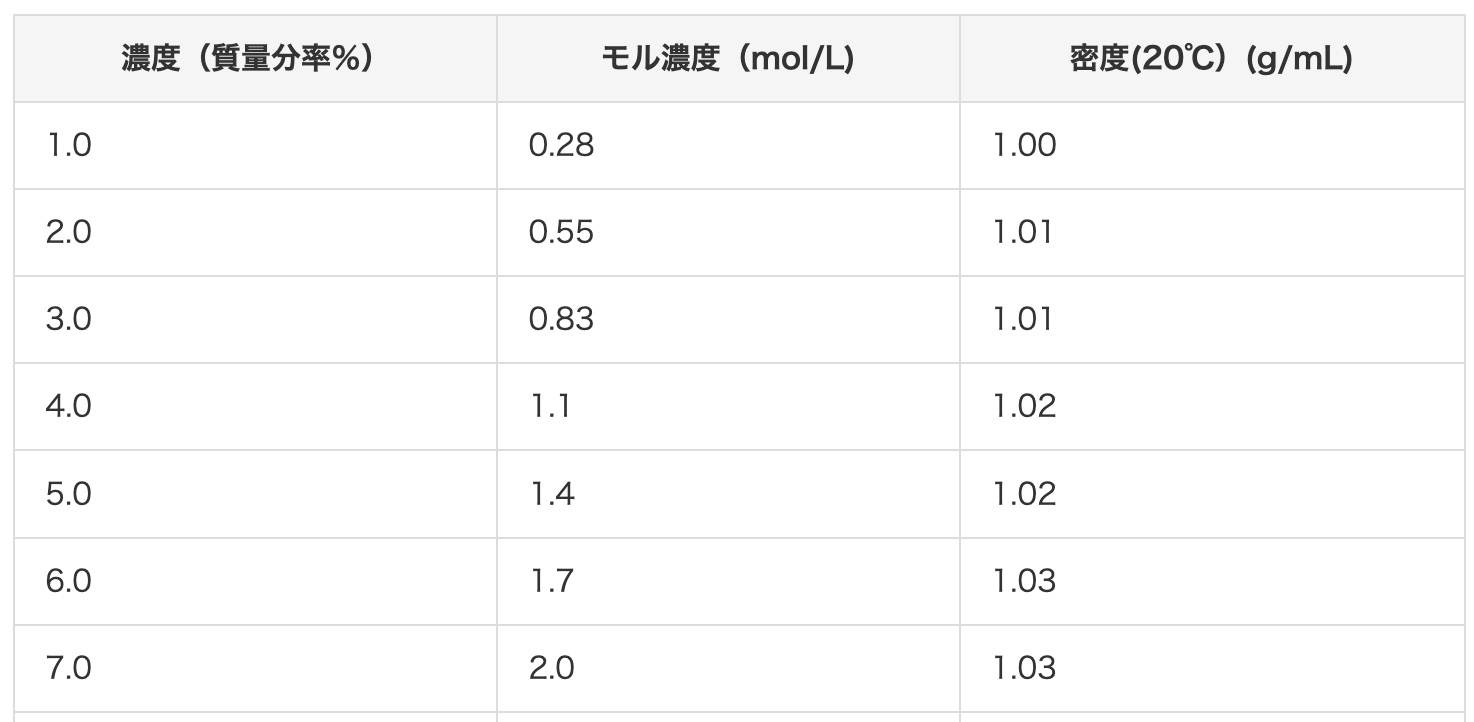
接下來,我們實際來試試看,把2 mol/L的鹽酸換算成質量百分濃度。據這個網站的對照表顯示,2 mol/L的鹽酸大約是7%。我們就來動手算算看是不是真的!
實戰演練!莫耳濃度換算成質量百分濃度
首先,要收集計算所需的資訊:鹽酸(HCl)的分子量:把原子量加起來。氫(H)是1,氯(Cl)是35.5,所以 1 + 35.5 = 36.5。鹽酸(2 mol/L)的密度:資訊顯示是1.03 g/cm³。這代表每1 cm³的體積,重量是1.03 g。
現在,我們以1公升的溶液為基準來計算。
溶質:2 mol ⟶ 2 × 36.5 = 73 g
溶液:1 L = 1000 cm³ ⟶ 1000 × 1.03 g/cm³ = 1030 g
我們知道了,1 L的溶液(1030 g)裡,溶有73 g的氯化氫。把這個數值代入質量百分濃度的公式…
73 (g) ÷ 1030 (g) = 0.070… 也就是約7%!
完美符合對照表上的數值!
反過來算!質量百分濃度換算成莫耳濃度
接著,我們來挑戰反向計算。只要一個單位一個單位慢慢換算,一定能成功!例如,我們來求濃度7%、密度1.03 g/mL的鹽酸,它的莫耳濃度是多少。莫耳濃度的重點是「1 L的溶液裡溶有多少莫耳的溶質」。
首先,計算1 L溶液的重量。
溶液 1 L = 1000 mL ⟶ 1000 mL × 1.03 g/mL = 1030 g
這裡面的7%就是溶質(氯化氫)的重量,所以:
溶質 1030 g × 0.07 = 72.1 g
最後,把這個溶質的重量換算成莫耳。除以氯化氫的分子量36.5,得到:
72.1 (g) ÷ 36.5 (g/mol) ≒ 1.97 (mol)
因為1 L的溶液裡有1.97 mol的溶質,所以濃度大約是2 mol/L。結果完全正確!
超好用的計算工具
對於常用的化學藥品,像是鹽酸和氫氧化鈉,已經有人幫我們寫好了濃度換算程式。你可以用這些工具來檢驗一下自己的計算有沒有錯。
https://keisan.casio.jp/menu/person/TaikiIkekame
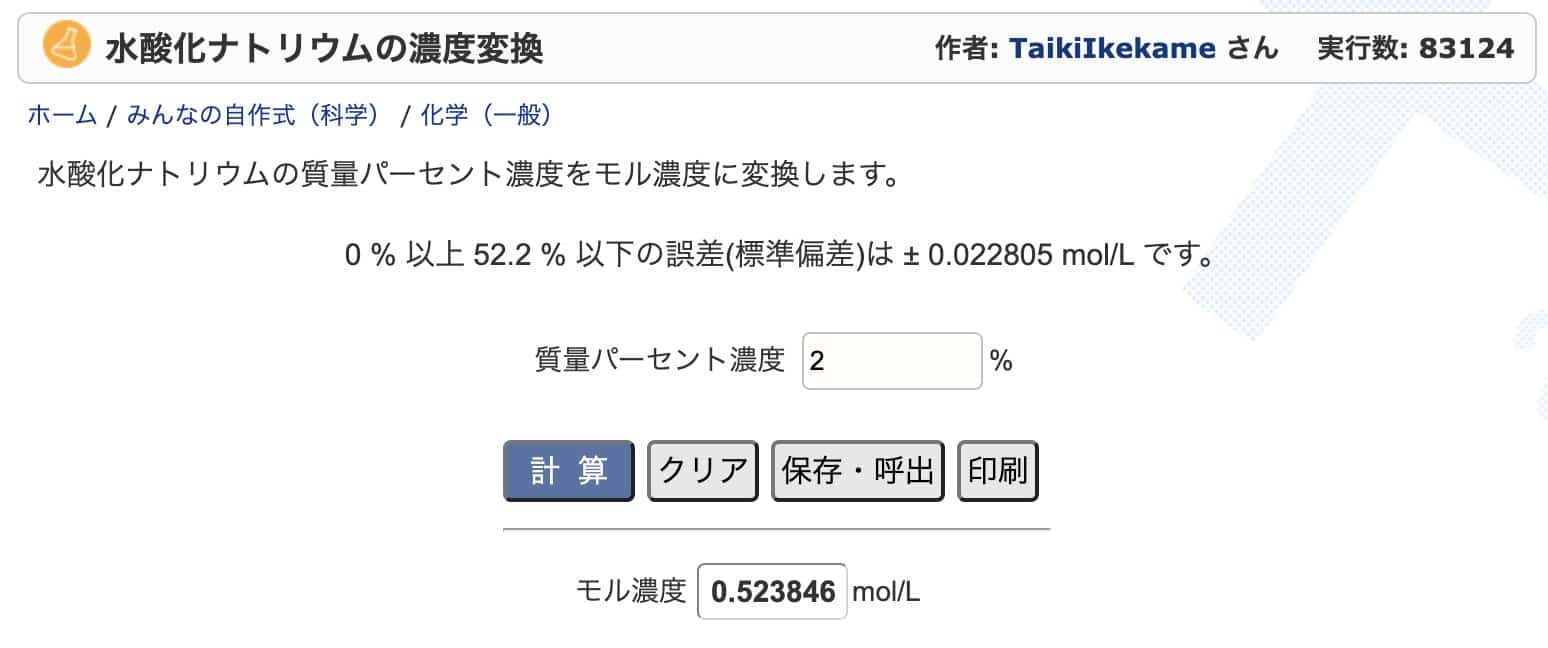
例如,在這個網站上輸入「7%」的鹽酸濃度,點一下計算,馬上就會得到精準的「1.981 mol/L」。
https://keisan.casio.jp/exec/user/1480248881

【小知識①】鹽酸和氯化氫有什麼不同?
這兩個常常被搞混。「氯化氫(HCl)」在常溫下是氣體。當這種氣體溶於水(水溶液)後,就變成「鹽酸」。其實,我們胃裡面的胃酸,主要成分也是鹽酸,負責幫助我們消化食物。記住囉,千萬不要把「氯化氫HCl」和「氯Cl」搞混了!
【小知識②】什麼是規定度(N)?
還有一種單位叫 「規定度(N)」 。它是在莫耳濃度的基礎上,再乘以該酸或鹼所帶有的「功力數(價數)」而得到的。例如,鹽酸(HCl)的功力是1(一價),所以1 mol/L的鹽酸,它的規定度也是1 N。而硫酸(H₂SO₄)的功力是2(二價),所以1 mol/L的硫酸,規定度就會變成2 N。這是一個能直觀比較酸或鹼反應強弱的方便單位。想了解更多,請看這裡。
【小知識③】ppm到底有多小?
「ppm」是「百萬分之一」的意思,是 “parts per million” 的縮寫。百分比是100分率,而ppm則是100萬分率。它專門用來表示非常非常微小的濃度。
溶質的質量(mg) / 溶液的質量(kg)
想像一下,在1 kg(1000 g)的溶液裡,只溶了1 mg的溶質,這個狀態就是1 ppm。

這到底有多小呢?舉個例子…
- 在1噸的重量中,只有1公克
- 在100萬元裡,只有1元
- 聽說在一個研討會上,有人說日本新年賀卡抽獎中,特獎的中獎機率大約就是1 ppm!(我查過了,是真的!)
這樣一想,是不是更能體會ppm是個多麼微小的比例了!
練習題:用氫氧化鈉來試試看
最後,讓我們用氫氧化鈉來練習一下。我們要把2%的氫氧化鈉水溶液換算成莫耳濃度。參考這張表,密度是1.02 g/mL(文章裡1.03g/mL是鹽酸的數據,所以我們用這個來算)。答案應該會是0.51 mol/L。
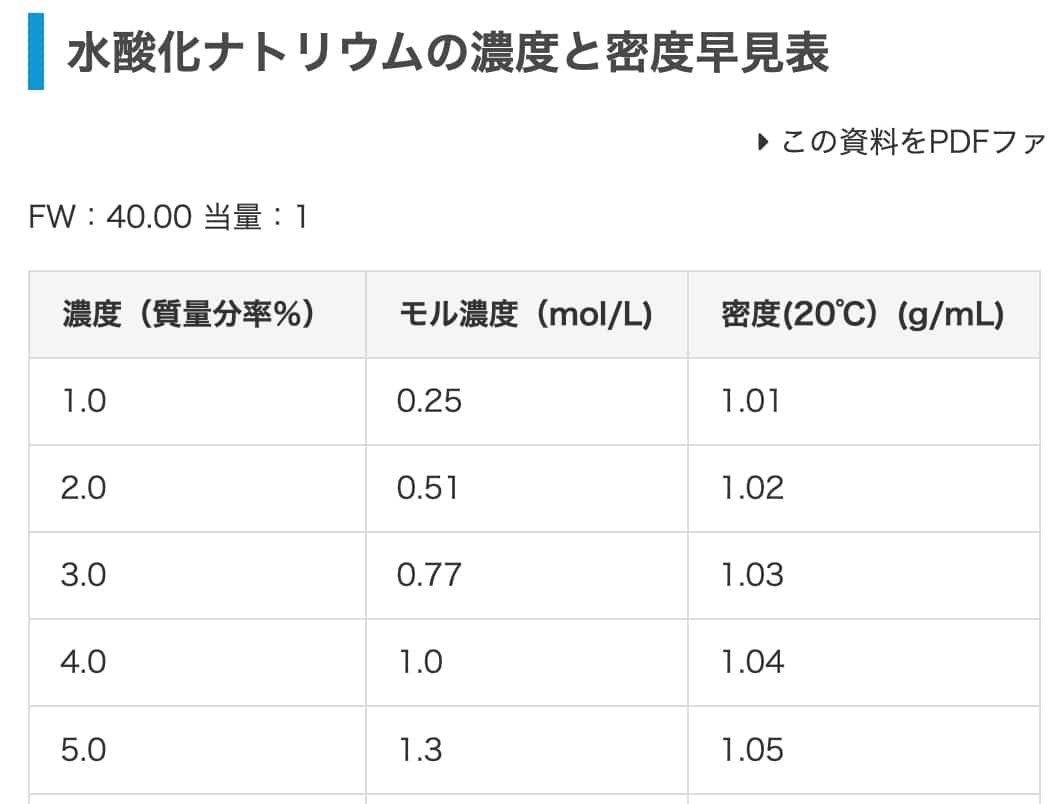
首先,計算1 L溶液的質量。
1000 mL × 1.02 g/mL = 1020 g
這其中的2%就是溶質的量,所以:
1020 g × 0.02 = 20.4 g
接著,把這個量換算成莫耳。氫氧化鈉(NaOH)的分子量是40,所以:
20.4 g / 40 (g/mol) = 0.51 mol
1 L的溶液裡有0.51 mol,所以莫耳濃度就是0.51 mol/L。和表上的答案完全吻合!
你也可以用這個網站來計算,結果幾乎一樣。
氫氧化鈉濃度換算:https://keisan.casio.jp/exec/user/1480256880
參考資料
國中常用的鹽酸,如果用濃鹽酸稀釋來用會很方便。例如,要配製10%的鹽酸,只要用體積比1:3.2的濃鹽酸和水混合即可。如果要把500 cm³的濃鹽酸全部配成10%,只需要加入1600 cm³的水。你可以把它們稀釋後存放在3公升的聚乙烯容器(amazon)裡,方便又安全。
|
|
聯繫我們・業務洽詢
讓科學的奧秘和樂趣更貼近生活!我們整理了許多在家就能做的有趣科學實驗和相關訣竅,快來多看看吧!
・關於經營者桑子研,請點這裡
・各種業務洽詢(寫作、演講、實驗課、電視節目監製、演出等),請點這裡
・文章更新資訊都在X上同步發布!
![]() 科學點子頻道正在發布實驗影片喔!
科學點子頻道正在發布實驗影片喔!
5月のイチオシ実験!
キーンと冷えるドライアイス!気温が上がってくるこの時期・ドライアイスを使った昇華・凝結・等速度直線運動の実験はいかが?

液体ゼロ!ドライアイスが消えるまでの3時間を科学する(昇華・凝結・等速度直線運動)
テレビ番組監修・イベント等のお知らせ
- 4月30日(木)「THE突破ファイル」(日本テレビ)の科学監修を担当しました。
- 5月8日(金)理科教育ニュースを担当しました。
- 6月14日(日) 千葉大学インスタレーション「探究」にて講師を務めます
- 6月26日(金) 千葉大学の公開研究会(中学理科について授業公開予定)
- 7月18日(土) 教員向け実験講習会「ナリカカサイエンスアカデミー」の講師をします。お会いしましょう。
書籍のお知らせ
- 『大人のための高校物理復習帳』(講談社)…一般向けに日常の物理について公式を元に紐解きました。特設サイトでは実験を多数紹介しています。※増刷がかかり6刷となりました(2026/02/01)

- 『きめる!共通テスト 物理基礎 改訂版』(学研)… 高校物理の参考書です。イラストを多くしてイメージが持てるように描きました。授業についていけない、物理が苦手、そんな生徒におすすめです。特設サイトはこちら。

各種SNS(更新情報をお届け!)
X(Twitter)/instagram/Facebook(日本語)
Explore
- 楽しい実験…お子さんと一緒に夢中になれるイチオシの科学実験を多数紹介しています。また、高校物理の理解を深めるための動画教材も用意しました。
- 理科の教材… 理科教師をバックアップ!授業の質を高め、準備を効率化するための選りすぐりの教材を紹介しています。
- Youtube…科学実験等の動画を配信しています。
- 科学ラジオ …科学トピックをほぼ毎日配信中!AI技術を駆使して作成した「耳で楽しむ科学」をお届けします。
- 講演 …全国各地で実験講習会・サイエンスショー等を行っています。
- About …「科学のネタ帳」のコンセプトや、運営者である桑子研のプロフィール・想いをまとめています。
- お問い合わせ …実験教室のご依頼、執筆・講演の相談、科学監修等はこちらのフォームからお寄せください。

![[商品價格如有變動,請以當下為準。] [商品價格如有變動,請以當下為準。]](https://hbb.afl.rakuten.co.jp/hgb/2c6a2576.25faaa1b.2c6a2577.0abda625/?me_id=1240371&item_id=10000489&pc=https%3A%2F%2Fthumbnail.image.rakuten.co.jp%2F%400_mall%2Fnagamineshouten%2Fcabinet%2Fporikan%2F3-1.jpg%3F_ex%3D80x80&s=80x80&t=picttext)